Ретиноиды (подробный обзор)
Акнекутан, Роаккутан, Сотрет
Акнекутан, Роаккутан, Сотрет
Системные ретиноиды содержат действующее вещество — изотретиноин. Это вещество применяется в мировой медицине почти 40 лет и является золотым стандартом лечения акне и угревой сыпи.
Что же это за вещество? Это трансретиноевая кислота и она очень мощно подавляет активность сальных желёз.
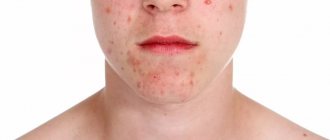
Когда возникает акне?
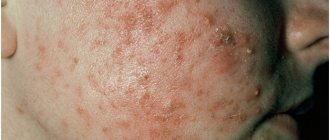
Акне возникает тогда, когда под воздействием избыточного воздействия гормона тестостерона на сальную железу, стимулируется мощная выработка кожного сала в большом количестве.
Как работают системные ретиноиды?
На рецепторы сальной железы воздействуют системные ретиноиды, присоединяясь к рецепторам сальной железы, они тормозят активность выделения сала из железы и акне проходит.
Самые, часто назначаемые препараты из системных ретиноидов (разрешены в Российской Федерации):
- Роаккутан
- Акнекутан
- Сотрет
Комментарий врача-косметолога, дерматолога Юлианы Шиян:
Когда я назначаю один из этих препаратов, меня спрашивают, а почему именно этот препарат и какая разница между ретиноидами? Все эти препараты объединяет одно вещество: Изотретиноин. Самый первый появился Роаккутан. Это оригинальный препарат, а все остальные препараты, это его *дженерики. Все дженерики изотретиноина имеют свои собственные регистрационные удостоверения и разрешены на территории России.
*ДЖЕНЕРИК — одобренная копия оригинального препарата
Роаккутан и Сотрет практически не отличаются друг от друга ни по формуле, ни по дозе. При их назначении, нет никакой разницы и выбор в пользу одного или другого — несущественный. Акнекутан содержит то же самое вещество, но его формула немного отличается от Роаккутана и Сотрета.
Почему Акнекутан более интересен врачу-косметологу и самому пациенту, как выбор для лечения и как понять, какой препарат из ретиноидов лучше?
Изотретиноин, это жирорастворимое вещество. Он усваивается организмом, только в сочетании с поглощаемыми жирами. Если вы принимаете Роаккутан и запиваете его обычной водой, он усвоится у вас менее, чем на 40%. Если вы принимаете Акнекутан и запьёте его обычной водой, он усвоится организмом примерно на 70%.
При назначении Акнекутана, врач страхует пациентов от их же собственных ошибок. Пациенты могут пренебречь жирной пищей во время приема Роаккутана и Сотрета, забудут съесть что-нибудь жирное или жирное им запрещено (на диете), а необходимая доза препарата должна попасть в организм! Необходимая, а не её малая часть! Поэтому препарат Акнекутан более предпочтителен для пациента, недобор по жирам при его приеме с меньшей вероятностью скажется на итоге лечения.
Его ежедневная доза регулируется врачом, но ещё есть кумулятивная дозировка препарата, которую должен накопить организм пациента. Именно при ее наборе мы можем говорить о большом шансе на стойкую ремиссию у пациента.
Из-за того, что Акнекутан усваивается лучше, производитель сделал чуть меньше действующего вещества в одной дозе, а значит: Рабочая доза — 20 мг. Роаккутана, соответствуют рабочей дозе Акнекутана с 16-ю миллиграммами Изотретиноина.
Вывод простой, если в организме накапливается меньше изотретиноина, то риски побочных явлений тоже снижаются. Это очень хорошо для пациента!
Для ярых сторонников всего оригинального и оригинальных препаратов в том числе, рекомендуется Роаккутан. Но и все другие ретиноиды будут для вас полезны, при условии, если они назначены врачом-дерматологом, а вы в свою очередь, будете соблюдать все условия приема ретиноидов.
Эффективность системных ретиноидов при акне
Акне (вульгарные угри) является одним из наиболее распространенных заболеваний кожи, которым на различных этапах жизни страдают до 90–95% населения земного шара [1]. При этом частота заболевания в возрасте 12–25 лет достигает 85%. При установлении этиологии и патогенеза акне определенную роль играют генетические и конституциональные особенности организма. Показано, что частота возникновения угрей у ребенка превышает 50%, если они присутствуют у обоих родителей [2, 3]. В результате последних исследований было установлено, что развитие акне происходит на фоне нескольких взаимосвязанных патогенетических механизмов. Наиболее значимыми из них являются: нарушение процессов кератинизации, патологический фолликулярный гиперкератоз, избыток продукции сального секрета, сопровождающегося дисбалансом липидов и размножением микроорганизмов [4–6]. В большинстве случаев акне рассматривается как конституционально детерминированное заболевание с повышенной чувствительностью себоцитов к андрогенным стимулам [7, 8]. Доказано, что интенсивность секреции кожного сала, величина и количество сальных желез, готовность к воспалительному процессу генетически обусловлены, однако генетические факторы могут играть важную роль в развитии заболевания сальных желез только в том случае, когда на генетическую предрасположенность наслаивается воздействие других факторов окружающей среды. Появление высыпаний при тяжелом течении акне может привести впоследствии к выраженным косметическим дефектам, наличие которых отрицательно влияет на психоэмоциональное состояние больных, снижает самооценку, вызывает депрессивные расстройства, приводит к социальной дезадаптации. Даже при легкой и средней степени тяжести вульгарных угрей у ряда пациентов отмечается психологичес-кий дискомфорт, наблюдаются повышенная ситуативная и личностная тревожность, различные виды нозогенных депрессий, чаще всего регистрирующиеся у женщин. 90% больных, страдающих акне, испытывают эстетический дискомфорт, 62% – имеют трудности в общении с другими людьми, 45% – отмечают сложности в работе или учебе [9]. Несмотря на известный во многом механизм развития вульгарных угрей, лечение по-прежнему представляет определенные сложности. Тактика лечения больных вульгарными угрями определяется клинической формой и тяжестью заболевания, возрастом и полом больного, сопутствующими заболеваниями, предшествующим лечением и его эффективностью, особенностями развития и течения рецидивов, их длительностью. При легком течении вульгарных угрей, как правило, назначается только наружная терапия и правильный уход за кожей, а при среднем и тяжелом течении – системная терапия, которая включает три основные группы препаратов (антибиотики, синтетические ретиноиды, гормональные препараты). Пероральные антибиотики назначают для подавления микробной колонизации. Антибиотики группы тетрациклинов, включающие доксициклин, тетрациклин, миноциклин, являются основными в схемах лечения акне, однако тетрациклин в настоящее время практически не применяется. В последнее время проблема развития резистентности к антибиотикам в результате длительного приема приобрела чрезвычайно актуальный характер. Чаще всего наблюдается устойчивость к эритромицину и клиндамицину. В прошлые годы развитие резистентных штаммов Propionibacterium acnes встречалось очень редко, тем не менее в настоящее время результаты многих исследований показывают, что более чем у 60% пациентов, получавших антибиотики курсом более 1 мес., развивается резистентность к эритромицину, причем вероятность развития резистентности к пероральному приему антибиотика так же велика, как и к наружному, в связи с чем не рекомендовано назначать антибиотики в виде монотерапии. Согласно Европейским рекомендациям в лечении вульгарных угрей средней и тяжелой степени целесообразно сочетать пероральный прием антибиотиков с наружными средствами, содержащими ретиноиды или бензоила пероксид, у женщин возможно их сочетание с гормональной терапией. Женщинам с гормональными нарушениями, рецидивирующими, устойчивыми к наружной терапии вульгарными угрями рекомендуется лечение половыми гормонами. Прием пероральных гормонов уменьшает секрецию кожного сала, ингибирует эффекты андрогенов в сальных железах. В целях лечения угревой болезни в основном используются три группы гормонов: эстрогены, которые подавляют овариальные андрогены; глюкокортикоиды, которые ингибируют надпочечниковые андрогены, и пероральные антиандрогены, которые действуют прежде всего на периферическом уровне. Эстрогены в небольших дозировках (35–50 мкг), применяемые в качестве пероральных противозачаточных средств, способны значительно снижать секрецию кожного сала. Лечение антиандрогенами проводится после консультации гинеколога-эндокринолога, при этом могут потребоваться оценка гормонального профиля крови (лютеинизирующий гормон, фолликулостимулирующий гормон, эстрадиол, прогестерон, тестостерон, пролактин и дегидроэпиандростерон-сульфат), УЗИ органов малого таза и надпочечников, рентгенография или томография черепа. Наиболее эффективными в терапии акне по-прежнему остаются системные ретиноиды, в частности изотретиноин. Препарат показан пациентам с узловато-кистозными угрями и с часто рецидивирующими воспалительными высыпаниями, у которых лечение антибиотиками было неэффективным, а также у больных с тенденцией к образованию рубцов; и спектр показаний для назначения изотретиноина расширяется. Изотретиноин, являясь комедонолитиком, действует на патологическую фолликулярную кератинизацию и уменьшает функцию сальных желез, обладает прямым антихемотаксическим и противовоспалительным эффектом. Несмотря на то, что изотретиноин не обладает прямым антибактериальным эффектом, он способен влиять на процесс хемотаксиса и фагоцитоза и таким образом уменьшать численность пропионбактерий [10]. Уже через 2 нед. после начала лечения изотретиноином отмечается уменьшение продукции кожного сала. Как следствие, рост микроорганизмов и провоспалительных медиаторов резко снижается, поэтому сегодня изотретиноин является единственным препаратом, который воздействует на большинство звеньев патогенеза акне. Это происходит благодаря молекулярным механизмам действия изотретиноина, который, взаимодействуя с ядерными рецепторами, уменьшает дифференцировку клеток сальных желез, что способствует выраженному уменьшению размеров и активности себоцитов. Известно, что изотретиноин в дозе 0,5–1,0 мг/кг в день значительно сокращает выделение кожного сала (на 80%) уже в течение 6 нед. после начала лечения. Препарат назначается на длительный срок – от 4 мес. до 1 года, в дозах от 0,1 мг/кг до 1 мг/кг массы тела в зависимости от тяжести заболевания. Обязательным условием является прием препарата во время еды. К сожалению, из-за страха развития побочных эффектов на фоне приема изотретиноина врачи не всегда своевременно назначают препарат. Обычно препарат вызывает опасения у врачей, у которых отсутствует опыт его применения. Бытует мнение, что после окончания лечения нельзя беременеть в течение 2-х лет, при этом изотретиноину ошибочно приписывается свойство других ретиноидов (этретината и ацитретина), имеющих в отличие от изотретиноина продолжительный период полувыведения. Вместе с тем период полувыведения изотретиноина составляет всего 19 ч, однако необходимо предохранение от беременности на весь период терапии и 1 мес. после ее окончания. Побочные явления действительно могут сопровождать курс лечения, но в большинстве случаев речь идет о хейлите и сухости кожных покровов. Другие побочные эффекты, такие как транзиторное изменение трансаминаз, головная боль, миалгии, ухудшение ночного зрения, описанные в инструкции по применению препарата, встречаются значительно реже и, как правило, не требуют прекращения лечения. С целью минимизации рисков развития побочных эффектов со стороны печени и поджелудочной железы при лечении изотретиноином производителями рекомендован постоянный мониторинг биохимических показателей крови (печеночные ферменты, холестерин и уровень триглицеридов): через 3–4 нед. после начала лечения, а затем 1 раз в 1–2 мес., при показаниях – чаще. Важно помнить, что рекомендована монотерапия изотретиноином. Одновременное применение с тетрациклинами должно быть исключено во избежание увеличения внутричерепного давления. Для лечения тяжелых форм акне на протяжении последних лет с успехом применяется препарат Акнекутан (производится по запатентованной в Бельгии технологии Lidose), действующим веществом которого является изотретиноин. Как известно, изотретиноин относится к плохо растворимым соединениям и усваивается в пищеварительном тракте не полностью. Технология Lidose заключается в добавлении 2-х дополнительных компонентов в состав каждой капсулы препарата Акнекутан (Гелюцир и Спан), благодаря которым увеличивается растворенная фракция изотретиноина в каждой капсуле, и препарат более полно усваивается в пищеварительном тракте по сравнению с обычной формой изотретиноина. Биодоступность увеличивается на 20% по сравнению с обычной формой изотретиноина, что и позволяет уменьшить количество изотретиноина в каждой капсуле на 20% с сохранением терапевтической эффективности препарата. Акнекутан выпускается в капсулах по 8 и 16 мг, которые биоэквивалентны капсулам по 10 и 20 мг с обычным изотретиноином. При этом из 16 мг Акнекутана в кровь поступает 12 мг изотретиноина, так же, как и из 20 мг обычной формы препарата, а количество неактивного изотретиноина сокращается в 2 раза (4 мг в Акнекутане и 8 мг в препаратах обычной формы изотретиноина). Это, в свою очередь, уменьшает вероятность развития побочных эффектов и улучшает переносимость препарата. Еще одним важным моментом является то, что биодоступность Акнекутана зависит от приема пищи гораздо меньше по сравнению с обычной формой изотретиноина. При приеме без пищи Акнекутан усваивается на 70%, в то время как обычная форма изотретиноина только на 38%. Таким образом, применение Акнекутана позволяет на 20% снизить количество поступающего в организм изотретиноина без ущерба для терапевтической эффективности препарата. Кроме того, случайные приемы препарата без пищи не приведут к снижению курсовой дозы изотретиноина. Рекомендуемая суточная доза Акнекутана составляет 0,4–0,8 мг/кг, а курсовая доза – 100–120 мг/кг массы тела. В связи с вышеизложенным хотим поделиться опытом применения Акнекутана у больных акне. Под нашим наблюдением в клинике кожных и венерических болезней им. А.В. Рахманова находились 46 больных: 25 (54,3%) мужчин и 21 (45,7%) женщина в возрасте от 15 до 38 лет с давностью заболевания от 2 до 23 лет. У 30 (65,3%) больных отмечалась средняя степень тяжести и у 16 (34,7%) – тяжелая. Степень тяжести заболевания определяли с помощью дерматологического индекса акне (ДИА) (Н.Г. Кочергин, Д.В. Игнатьев, 2004) путем подсчета количества образований на коже – папул, пустул и узлов [11]. У больных со средней степенью тяжести значение ДИА соответствовало 7,59±1,12 балла, а с тяжелой степенью – 11,32±1,43 балла. Анамнестически установили, что пациенты в прошлом лечились различными методами с многократными курсами, включающими системные антибиотики, метронидазол, антиандрогены, наружные средства, чистки, пилинги и др., однако лечение давало лишь временный клинический эффект. Лечение Акнекутаном проводили после обследования (клинический и биохимический анализ крови), из расчета 0,4–0,8 мг/кг в сутки во время еды. Для нивелирования явлений ксероза и хейлита все пациенты применяли увлажняющий крем для сухой и чувствительной кожи 2–3 раза в день и увлажняющие губные помады. При достижении выраженного улучшения клинической картины суточная доза Акнекутана постепенно снижалась, и при наборе кумулятивной дозы от 100 до 120 мг/кг (114,5±4,4 мг/кг) лечение прекращали. В результате проведенной терапии отмечалась 100% редукция ДИА у больных акне средней степени тяжести, т. е. была достигнута клиническая ремиссия. При тяжелой степени редукция ДИА составила 94%, что соответствовало почти полной клинической ремиссии (рис. 1, 2 ).
В процессе терапии пациенты отмечали сухость губ (46 больных – 100%) и лица (34 больных – 74%) в той или иной степени выраженности, особенно в первые месяцы терапии. Если сухость лица у большинства больных купировалась применением увлажняющего крема для сухой и чувствительной кожи, то хейлит, несмотря на использование увлажняющих губных помад, сопутствовал всему курсу терапии Акнекутаном, однако ни один пациент не изъявил желания прекратить лечение, видя впечатляющий клинический эффект от Акнекутана. Одна пациентка на 5-м месяце приема Акнекутана предъявила жалобы на артралгии, которые полностью разрешились в течение 3 нед. после лечения нестероидными противовоспалительными препаратами. При ежемесячном контроле биохимических показателей крови у 22 (48%) больных отмечались незначительные изменения (менее 20%) показателей триглицеридов, липопротеидов высокой и низкой плотности и коэффициента атерогенности, которые полностью приходили в норму после окончания лечения. Перечисленные побочные явления не требовали отмены препарата. При опросе все пациенты сообщили, что лечение переносили хорошо. Таким образом, наш многолетний опыт показал, что Акнекутан является высокоэффективным препаратом для лечения средней и тяжелой степени акне, его эффективность соответствует оригинальному препарату изотретиноина, но при этом Акнекутан имеет преимущество по переносимости лечения перед препаратами обычных форм изотретиноина [12], а также более удобен для пациентов с точки зрения меньшей зависимости приема препарата от пищи. Как правило, системная терапия изотретиноином приводит к выздоровлению или значительному улучшению состояния кожи пациентов с акне, а также обеспечивает длительную ремиссию заболевания. Однако в ряде случаев (10–25%) может потребоваться повторный курс терапии, проведение которого возможно не ранее чем через 8 нед. после окончания предыдущего курса лечения. Рецидив может быть связан с отсутствием коррекции сопутствующих заболеваний, играющих важную роль в патогенезе акне. Поэтому перед началом лечения важно исключить такие состояния, как поликистоз яичников, заболевания щитовидной железы, нарушения толерантности к углеводам, врожденную гиперплазию коры надпочечников. Кроме того, преждевременное прекращение лечения Акнекутаном без достижения кумулятивной дозы 100–120 мг/кг также может способствовать развитию рецидивов.
Ретинол и третиноин
Чтобы повысить эффективность лечения, можно применять лекарственные крема и мази, содержащие не ретинол, а чистую ретиноевую кислоту — третиноин. Препарат с третиноином по сравнению с препаратом с ретинолом при меньшей в несколько раз концентрации оказывает столь же эффективное воздействие на кожу, при повышении концентрации (до разумного предела) его лечебное действие усиливается. Но при этом у некоторых людей могут наблюдаться побочные эффекты в виде аллергических реакций на чистый третиноин — легкий зуд, шелушение и т.д. Эти эффекты проходят по мере того, как организм привыкает к препарату. О побочных эффектах можно почитать здесь.
Побочные эффекты от лечения системными ретиноидами
Терапию системными ретиноидами нужно проводить только под контролем специалиста. Принимая эти препараты, необходимо раз в месяц сдавать биохимический анализ крови: проходить проверку уровня печеночных ферментов (АЛТ, холестерина, щелочной фосфатазы, АСТ, триглицеридов). Если указанные показатели растут, специалист может снизить дозу лекарства. Если наблюдается повышение триглицеридов и есть жалобы на работу печени, ЖКТ, необходимо дополнительно провести проверку уровня липазы и амилазы, чтобы вовремя обнаружить панкреатит44.
При лечении прыщей* ретиноидами следует прекратить потребление алкоголя и использовать солнцезащитные средства. Нельзя сочетать лекарство с тетрациклином, так как оба средства способны повысить внутричерепное давление44.
Ретиноиды могут вызвать такие побочные эффекты44:
- хейлит;
- сухость кожи;
- конъюнктивит,
- сухость слизистых;
- повышение фоточувствительности;
- ухудшение ночного зрения;
- головные боли;
- миалгии, артралгии;
- транзиторное выпадение волос.
Наиболее частой ситуацией, настораживающей пациентов в начале лечения системными ретиноидами, является так называемый ретиноевый дерматит. Он развивается спустя примерно, когда в крови достигается определенная кумулятивная доза препарата. Такая реакция считается нормальной. Появляются раздражения, покраснение кожи, особенно в местах, где она тонкая. Может ощущаться зуд и повышенная чувствительность.29
Побочные эффекты прекращаются после окончания приема препаратов. В первые 30-60 дней возможно обострение симптомов. Крайне не рекомендуется самостоятельно снижать дозировку или прекращать прием лекарств, необходимо обратиться к специалисту, который при необходимости скорректирует курс терапии44.